Abstract
In healthy skin keratinocytes provide the essential function of self-renewing themselves, regularly communicating with each other, with dermis and the immune system by a delicate balance of biochemical signals and cellular responsiveness, which slow down during the aging and photoaging phenomena.
The main goal of Cosmetic Dermatology is to formulate Clinically Correct Cosmetics based on the use of effective and safe natural active ingredients and carriers, skin and environmentally friendly.
It has been shown by different studies that nanochitin-hyaluronan (CN-HA) and nanochitinlignin (CN-Lignin) block copolymeric nanoparticles may contemporary act as active carriers and ingredients ameliorating the skin sensible and prematurely aged. On one side they entrap into their
structure and load different active ingredients, such as, for example, antioxidant and immunomodulant compounds, releasing them at the right skin site at the right time. On the other side they are metabolized from the enzymes to glucosamine, acetyl glucosamine, glucose, hyaluronic acid (CN-HA) or to polyphenols (CN-lignin), and used from the skin cells as raw material and energy useful to repair their damages, caused from the environment and the aging processes. The paper reports some example of the results obtained in vitro and in vivo byte use of CN-HA and CN-Lignin, entrapping different active ingredients, to produce innovative Cosmetics and advanced medications.
Riassunto
Nella cute sana i cheratinociti svolgono la funzione essenziale di un loro continuo rinnovo, svolto attraverso l’uso di segnali intercellulari interscambiati dell’epidermide con il derma e con il sistema immunitario. La produzione di questi segnali rallentano con l’invecchiamento della pelle aggredita dall’ambiente.
Il principale scopo della Dermatologia Cosmetologica è di formulare cosmetici clinicamente corretti basati sull’uso di ingredienti e veicoli, possibilmente naturali, efficaci, privi di effetti collaterali e rispettosi sia della cute che dell’ambiente.
Diversi studi hanno posto in evidenza come i complessi naturali nanochitina-acido ialuronico e nanochitina- nanolignina siano, in grado di agire come veicoli e principi attivi apportando benefici alla cute sensibile e precocemente invecchiata. Questi complessi innovativi da una parte intrappolano e trasportano diversi ingredienti attivi, quali ad esempio antiossidanti e immunomodulanti, cedendoli ai giusti siti cutanei nei tempi prestabiliti. Dall’altra parte, vengono metabolizzati da appositi enzimi a glucosammina, acetil glucosammina, glucosio e acido ialuronico, CN-HA, o a polifenoli, CN-lignina, per essere utilizzati dalle cellule come materiale ed energia necessari per riparare i danni cutanei provocati dall’ambiente e dai processi di invecchiamento.
Lo studio riporta alcuni esempi dei risultati sperimentali ottenuti, in vitro ed in vivo, dall’uso di questi
nuovi principi attivi naturali utilizzati per produrre cosmetici innovativi e medicazioni avanzate.
Introduzione
La pelle, composta dai diversi strati protettivi dell’ epidermide, del derma e dell’ipoderma, si comporta come una barriera biologica proteggendo l’organismo dall’aggressione continua esercitata dall’ambiente (Fig. 1)(1, 2).
Mentre lo strato corneo (SC), formato da più strati di corneociti, rappresenta la prima e più esterna barriera dell’epidermide, il derma organizzato con una matrice extracellulare (ECM), neutralizza lo stress ossidativo ed i processi infiammatori (3, 4). Per svolgere il proprio ruolo difensivo i corneociti, pieni di filamenti di cheratina sono racchiusi dentro una membrana proteica, circondati da una struttura lipidica lamellare organizzata in strati regolari composta da: cerammidi (~50%), colesterolo (~25%) e acidi grassi liberi (~15%) nel rapporto equimolecolare 1:1:1 (5, 6). Questi filamenti sono aggregati con enzimi, tra cui la filaggrina che, degradandosi durante il processo di rinnovo cellulare, dà luogo alla formazione dei fattori naturali di idratazione, i cosiddetti NMF, mantenendo anche costante il pH acido della cute (Fig. 2).
Legati alla membrana proteica del corneocita sono presenti diversi lipidi che sembrano agire da precursori delle lamelle. Così, da una parte i corneociti rappresentano un importante componente necessario a mantenere sia l’integrità meccanica della cute che l’omeostasi della barriera, attraverso il controllo dei processi di idratazione superficiale, di desquamazione e dei fenomeni infiammatori. Dall’altra parte, il collagene e le fibre elastiche, sintetizzate dai fibroblasti del derma come parte strutturale del’ECM, conferiscono alla pelle morbidezza, elasticità ed idratazione profonda. Così, l’integrità sia dei corneociti che dell’ECM risultano essenziali per proteggere e mantenere sana la pelle, salvaguardandola dalle continue aggressioni ambientali. Infatti, l’integrità cutanea dipende dagli specifici segnali intercellulari e dai legami che si stabiliscono tra i corneociti e l’ECM, dal ricambio regolare di queste cellule che da cheratinociti si trasformano in corneociti, oltre che dalla loro capacità di contrastare l’aggressività dei radicali liberi, modulare i processi infiammatori e permettere il regolare svolgersi del meccanismo della mutagenesi (7).
Con il processo dell’invecchiamento si verificano diversi fenomeni tra i quali predominano, l’assottigliamento dello strato corneo, accompagnato da variazioni della perspiratio insensibilis (TEWL), da un graduale declino delle funzioni immunologiche e da una ridotta risposta agli allergeni. A questi fenomeni si accompagnano processi infiammatori cutanei che si acuiscono notevolmente se paragonati alla reattività di una cute giovane (8-10). Per questi motivi anche i cheratinociti, collegati con la lamina basale attraverso la struttura degli emo-desmosomi glicoproteici, debbono essere protetti nei loro processi e meccanismi molecolari per permettere loro di migrare e proliferare. Da parte sua, la struttura cellulare del derma, risulta necessaria per mantenere e proteggere la trasmissione dei continui messaggi intercellulari, tra cui la MAPK (Mitogen Activated Protein Kinase) e la NF-kB (Nuclear Factor kB) (11). Come conseguenza di questa continua attività, l’espressione dei geni e delle proteine dell’ ECM debbono essere rigenerate, perché continuamente alterate dagli stress ossidativi e dai processi infiammatori. Infatti, l’apparire e il formarsi delle rughe, che appaiono con l’invecchiamento, sono fenomeni strettamente collegati con l’alterata differenziazione e il discontinuo rinnovo dei cheratinociti e delle lamelle lipidiche (12), fenomeni collegati tutti con una compromessa e ridotta espressione genica e una alterata sintesi sia delle fibre di collagene che di elastina. Inoltre, la continua esposizione alle radiazioni solari, accompagnata dal consumo di sigarette e dall’esposizione al vento e alle sostanze chimiche ambientali provoca una incrementata formazione di rughe e iperpigmentazioni cutanee, con un conseguente rilassamento e ridotta elasticità dei tessuti (Fig. 3) (13,14). Il collagene viene, infatti, degradato dalle metalloproteinasi, mentre l’incrementata presenza dei radicali liberi, esaltata dall’eccessiva esposizione ai raggi solari, provoca danni a livello dei lipidi, delle proteine e degli acidi nucleici.
Per tutti questi motivi, la cute protegge se stessa attraverso la produzione di antiossidanti, quali le vitamine C ed E che, come donatori di elettroni, neutralizzano in parte l’attività svolta dai radicali liberi (Fig. 4) (15-17). Inoltre, sembra che l’attività enzimatica svolta dalle proteasi sia in grado di facilitare il movimento dei cheratinociti rimodellandone la parte proteica presente nell’ECM, producendo ed attivando i segnali intercellulari e stabilizzando citochine e fattori di crescita (18). Il giusto equilibrio tra antiossidanti e proteasi è considerato, infatti, cruciale per risolvere sia i problemi legati ai processi infiammatori troppo prolungati, che per regolarizzare la produzione dei corneociti, essenziali per mantenere integra l’intera struttura cutanea (Fig. 4).
In conclusione, il normale funzionamento della pelle dipende direttamente dall’organizzazione delle lamelle lipidiche, dallo spessore dello strato corneo, determinato dal numero dei corneociti, dalla loro dimensione e coesione, e dalla regolare organizzazione dell’ECM (19, 20).
Cosmesi Dermatologica e Invecchiamento Cutaneo
Come descritto, nella cute sana i cheratinociti, come tutte le cellule specializzate, svolgono i loro precisi compiti di rinnovare continuamente l’epidermide, regolando questa funzione attraverso i continui messaggi che scambiano tra di loro, con il derma ed il sistema immunitario (21). Pertanto, il coordinato sistema epidermico di continua degradazione e rigenerazione delle proprie cellule richiede un delicato bilanciamento dei loro messaggi biochimici in entrata e in uscita, che purtroppo si riducono con i processi di invecchiamento (22). Infatti, i cheratinociti basali dell’epidermide, i follicoli dei capelli, e la produzione del sebo dei dotti pilo-sebacei debbono difendersi dalle continue aggressioni e dai processi di invecchiamento dell’ambiente e rinnovarsi di continuo attraverso i regolari processi di rigenerazione cellulare mediati dalla produzione dei fattori di crescita, delle citochine e delle chemiochine.
Lo scopo principale della cosmesi dermatologica è di formulare prodotti clinicamente corretti basati sull’uso di ingredienti e veicoli naturali affini sia alla pelle che all’ambiente. Questi cosmetici innovativi debbono essere in grado di controbattere e ridurre i fenomeni legati all’ invecchiamento, minimizzando anche eventuali fenomeni di allergie e sensibilizzazioni cutanee. Gli ingredienti attivi utilizzati per i cosmetici debbono essere in grado di regolare sia la produzione dei lipidi intercellulari (lamelle lipidiche) che la sintesi degli NMF, mediante una rinnovata e modulata sintesi della filaggrina (23, 24). Come conseguenza si otterrà una regolazione della idratazione cutanea che porterà ad un regolare ricambio dei corneociti e ad una normalizzazione della barriera cutanea (Fig. 5). La contemporanea e regolare attività dei fibroblasti contribuirà a produrre la giusta produzione di collagene, indispensabile per ristabilire una cute salubre e più giovane (25, 26). Comunque, è importante sottolineare come nelle formulazioni cosmetiche risultino di fondamentale importanza per la loro efficacia e sicurezza d’uso non soltanto gli ingredienti attivi selezionati ma anche e soprattutto il veicolo utilizzato.
Efficacia Del Veicolo
Il veicolo, se ben formulato, potrebbe anche svolgere una sua propria attività a livello topico, oltre ad essere in grado di trasportare e cedere gli ingredienti attivi alle giuste aree cutanee, nelle giuste dosi e nei tempi programmati (27). Ne rappresenta un esempio sia la nano-chitina che il nano-chitosano che trovano applicazioni in diversi settori di estremo interesse scientifico-applicativi: dal trasporto di farmaci e geni, alla produzione di speciali sensori utilizzati per ottenere immagini utili e indispensabili per una più corretta diagnosi o alla realizzazione di veicoli specializzati per il trasporto di farmaci utilizzati per il trattamento di alcune patologie gravi, quali le manifestazioni tumorali (28). Infatti, la chitina ed il chitosano, utilizzati nella loro dimensione nano e opportunamente modificati nella loro struttura, assumono caratteristiche profondamente diverse, se paragonate alle molecole originarie . Assumendo, infatti, particolari proprietà chimico-fisiche, quali una grande superficie, una maggiore porosità, una maggiore resistenza meccanica, ed un ottima conduttività elettrica e fotoluminescenza (29). Ad esempio, 1 gr di nanofibrille di chitina (CN) sviluppano una superficie di circa 400 mq, mentre la normale chitina, a parità di peso, sviluppa soltanto 2 mq (30). CN, inoltre, ha dimostrato di possedere una notevole capacità idratante, essendo in grado di legare attorno a se molte molecole di acqua (più di 3 trilioni per ml !), oltre ad essere in grado di agire come veicolo, trasportando e cedendo alla cute gli ingredienti attivi intrappolati nelle proprie nanoparticelle (31-33).
A tal riguardo è interessante evidenziare come il complesso nanochitina-nanolignina (Fig. 6), ottenuto dal nostro gruppo sotto forma di povere sottile mediante la tecnica combinata della “gelazione” e dello spray dryer, abbia evidenziato di potenziare notevolmente le interessanti attività’ biologiche svolte dalle nanofibrille di chitina utilizzate tal quali (34-36). Così le micro/nanoparticelle, ottenute complessando il polimero CN a carica positiva con le macromolecole di lignina a carica negativa, hanno posto in evidenza di essere in grado di incapsulare ingredienti attivi sia idrosolubili che liposolubili e di rilasciarli nelle aree cutanee a cui erano predestinate, nei tempi e nei dosaggi programmati (37). L’interessante efficacia biologica esercitata da questo veicolo binario è certamente dovuta alle attività proprie delle due diverse strutture molecolari. Questo speciale carrier è formato da una parte da CN, polimero della dimensione media di 240x 7×5 nm che, composto da circa 25 molecole di glucosammina e acetil glucosammina possiede una struttura simile all’acido ialuronico (Fig. 7)(38). Per le sue peculiari caratteristiche questo polimero naturale, oltre ad esercitare un’attività idratante, sembra in grado di modulate la sintesi e l’organizzazione dei lipidi cutanei rappresentati dalle cosiddette lamelle (40). Inoltre, essendo CN ricco di gruppi acetilici, è facilmente riconosciuto e metabolizzato dalle chitotriosidasi espresse dai macrofagi umani (41, 42). Come conseguenza la glucosammina e l’acetil glucosammina possono essere utilizzate, per esempio, per riparare le cartilagini o per sintetizzare i glicosamminoglicani dell’ECM, mentre l’eventuale produzione di glucosio potrà servire per l’attività energetica esplicata dai mitocondri. Dall’altra parte, la lignina (LG) con la sua dimensione media di 270 nm e la sua attività antimicrobica, antiossidante e protettiva nei confronti degli UV, potrebbe essere catabolizzata fino a produrre polifenoli, utili per potenziare le difese antiossidanti della cute (43, 44), o per incrementare l’attività fotoprotettiva esercitata dai filtri naturali della pelle o dai prodotti solari formulati (45). In questo modo CN-LG agirebbe contemporaneamente come veicolo e ingrediente attivo, utile anche per rinforzare l’attività idratante della cute attraverso la favorita sintesi della filaggrina.
Gli Ingredienti attivi
Numerosi studi hanno posto in evidenza come le nanoparticelle di CN, dei complessi CN-acido ialuronico (CN-HA) e CN-lignina (CN-LG) possano incapsulare o intrappolare diverse tipologie di ingredienti attivi, incrementando la loro efficacia e riducendone i possibili effetti collaterali (46-48). Infatti, CN ha dimostrato la capacità di formare nanoparticelle con zinco piritione o piritione olamina, incrementandone l’efficacia come ingredienti anti-forfora (Fig. 8) (49); di complessare gli ioni zinco trasportandoli e legandoli sulla superficie delle tegole cheratiniche, migliorando la luminosità dei capelli esposti all’azione dannosa degli UV (Fig. 9) (50) ed accelerandone la riparazione mediante aminoacidi e peptidi depositati nella loro zona corticale danneggiata (Fig. 9) (50); inducendo la regolare sintesi del collagene a livello della cute danneggiata, per evitare la formazione delle cicatrici ipertrofiche o dei cheloidi (Fig. 11) (51).
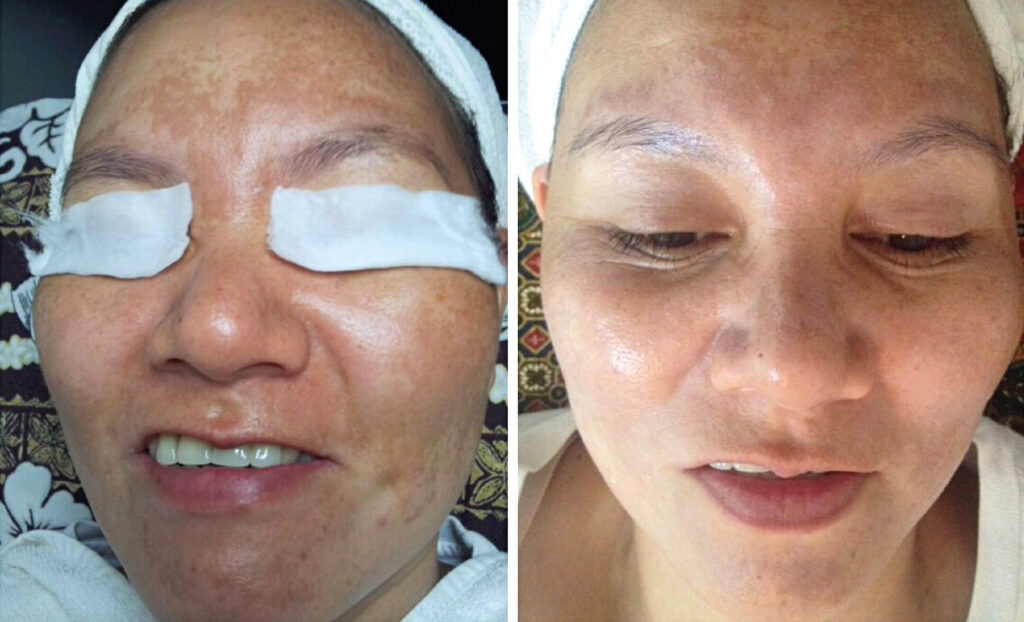
Da parte sua il complesso CN-HA ha anche dimostrato di poter modulare sia la produzione delle metalloproteinasi che delle collagenasi (Fig.12) (52, 53); di incrementare il potere antiossidante dei derivati della vitamina C (Fig.13)(54); di ridurre la sintesi della melanina ed il suo trasporto ai cheratinociti mediante i melanosomi, favorendo l’attività depigmentante dei prodotti cosmetici formulati come sbiancanti cutanei (Fig. 14)(54). Dall’altro lato, il complesso CN-lignina ha dimostrato di favorire la sintesi dei peptidi protettivi, conosciuti come defensine (Fig. 15)(55), esaltando anche l’attività riparativa della nicotinammide e l’attività protettiva dei filtri solari UVB-UVA (56).
Conclusioni
Come osservazioni conclusive è interessante ricordare come i polimeri naturali chitina e lignina, ottenuti rispettivamente da rifiuti industriali ed agricoli e perciò classificati come ingredienti verdi, risultino non soltanto biodegradabili e biocompatibili al 100%, ma siano anche considerati materie prime utili per salvaguardare l’equilibrio dell’ambiente e la biodiversità del nostro pianeta. Infatti, con il loro uso si ridurrebbe il consumo delle materie prime naturali, indispensabili per le future generazioni e per il mantenimento della biodiversità del nostro pianeta (Fig. 15)(57-59).
Inoltre, l’uso di questi nanoveicoli naturali e particolarmente innovativi dà la possibilità di poter incrementare l’efficacia degli ingredienti attivi selezionati, trasportandoli e cedendoli ai giusti siti, nel giusto dosaggio e nei tempi prestabiliti. In questo modo sarà possibile incrementare la loro biodisponibilità, incrementandone anche l’efficacia e l’accettabilità da parte dei pazienti e riducendone, infine, i possibili effetti collaterali.
- SECONDA UNIVERSITÀ DI NAPOLI
Docente di farmacologia cutanea, istituto di Dermatologia;
Visiting Professor, China Medical University, Shenyang
** Centro Ricerche, ISCD, Roma
Bibliografia
1) Elias PM, Choi EH. (2005) Interactions among stratum corneum defensive functions. Exp. Dermatol., 14: 719-726.
2) Proksch E, Brandner JM, Jensen JM. (2008) The skin: an indispensable barrier. Exp. Dermatol., 17: 1063-1072.
3) van Smeden J, Janssens M, Goris GS, Bowstra JA. (2014) The important role of stratum corneum lipids for the cutaneous barrier function. Biochim. Biophys. Acta, 841: 295-3013.
4) Wilhelm K, Brandt M, Maibach HI. (2004) Transepidermal water loss and barrier function of aging human skin. In: Fluhr IW, Elsner P, Berardesca E, Maibach HI (Eds): Bioengineering of the skin: Water and Stratum Corneum, Ed 2.Boca Raton, CRC-Press, pp 143-158.
5) Weerheim A, Pontec M. (2001) Determination of stratum corneum lipid profile by tape stripping in combination with high-performance thin-layer chromatography. Arch. Dermatol. Res, 293: 191-199.
6) Feingold KR, Elias PM. (2014) Role of lipids in the formation and maintenance of the cutaneous permeability barrier. Biochim. Biophys. Acta, 1842: 289-294.
7) Jacobo HT. (2003) The mitochondrial theory of aging: dead or alive? Aging Cell, 2:11-17.
8) Jafferany M, Huynh TV, Silverman MA, Zaidi Z. (2012) Geriatric dermatoses: a clinical review of skin diseases in an aging population. Int. J. Dermatol., 51: 509-522.
9) Rawling AV, Voegeli R. (2013) Stratun corneum protrasse and dry skin conditions. Cell Tissue Res, 351:217-235.
10) Danby SG. (2016) Biological Variations in Skin Barrier Function: From A (Atopic Dermatitis) to X (Xerosis). In: T Agner Ed, Skin Barrier Function, New York, Karger, pp 47-60.
11) Reichelt J, Furstenberger G, and Magin TM. (2004) Loss of keratin 10 to mitogen-activated protein kinase (MAPK) activation, increased keratinocyte and decreased tumoUr formation in mice. J. Invest. Dermatol., 123(5): 973-981.
12) Yuspa SH, Hennings H, Tucker RW, Jaken S, Kilkenny AE, and Roop DR. (2006) Signal Transduction for Proliferation and differentiation in keratinocytes. Ann. New York Acad Sci., 548(1): 91-196.
13) Berneburg M, Plettenberg H, Krutmann J. (2000) Photoaging of human skin. Photodermatol. Photoimmunol. Photomed., 16: 239-244.
14) Frances C. (1998) Smoker’s wrinkles: epidemiological and pathogenic considerations. Clin. Dermatol., 16: 565-570
15) Sies H. (1993) Strategies of antioxidant defense. Eur. J. Biochem., 215: 213-219.
16) Liebler DC. (1993) The role of metabolism in the antioxidant function of vitamin E. Crit. Rev. Toxicol., 23: 147-169.
17) Weber P, Bendich A, Schalch W. (1996) Vitamin C and human health – a review of recent data relevant to human requirements. Int. J. Vitam. Nutr. Res, 66: 19-30.
18) Ridley AJ, Schartz MA, Burridge K, Firtel RA, Ginsberg MH, Borisy G, Parson JT, and Horwitz TZ. (2003) Cell Migration: Integrating Signals from Front to Back. Science, 302: 1704-1709.
19) Hansen S, Naegel A, Heising M, Wittum G, Neumann D, Kostka KH, Meiers P, Lehr CM. and Schaefer UF. (2009) The role of corneocytes in skin transport revised. A combined computational and experimental approach, Pharm. Res, 26: 1379-1397.
20) Hadgraft J, Lane ME. (2009) Trasepidermal water loss and skin site: a hypothesis. Int. J. Pharm., 373:1-3
21) Harding PM. (2005) Interactions among stratum corneum defensive functions. Exp. Dermatol., 14: 719-726.
22) Elias PM. (2005) Stratum corneum defensive functions: an integrated view. J. Invest. Dermatol.,125: 183-200.
23) McAleer MA, Irvine AD. (2913) The multifunctional role of filaggrin in allergic skin disease. J. Allergy Clin. Immunol., 131: 280-291.
24) Kawasaki H, Nago K, Kubo A Hata T, Shimizu A, Mizuno, H Yamada T and Amagai M. (2012) Altered stratum corneum barrier and enhanced percutaneous immune responses in filaggrin-null mice. J. Allergy Clin. Immunol., 129: 1538e6-1546e6.
25) Morganti P. and Chen Hong-Duo (2011) Una emulsione innovativa per il trattamento della xerosis cutanea e dell’alterazione della barriera. Cosm. Technol., 14(4): 31-39.
26) Morganti P, Fabrizi G, Guarneri F, Palombo M, Cardillo A, Ruocco E, Del Ciotto P. (2011) Repair Activity of Skin Barrier by Chitin-Nanofibrils Complexes, SOFW-Journal, 13(5): 10-26.
27) Wiechers JW. (2008) Skin Delivery: What it is and Why we need it. In: JW Wiechers, (Ed) Science and Applications of Skin Delivery Systems, Carol Stream, IL, ALLURED Global Information Leader., pp 1-21.
28) Priya MV, Sabitha M. and Jayakumar R. (2016) Colloidal chitin nanogels: A plethora of applications under one shell. Carbohydrate Polymers, 136: 609-617.
29) Hamidi M, Azadi A. and Rafiei P. (2008) Hydrogel nanoparticles :From controlled release to pay-responsive drug delivery. Drug Discovery Today, 7: 569-579.
30) Morganti P. and Morganti G. (2008) Chitin nanofibrils for Advanced Cosmeceuticals. Clinics in Dermatology, 26(4): 334-340.
31) Morganti P, Palombo M, Palombo P, Fabrizi G, Cardillo A, Morganti G, Ruocco E, and Dziergowski S. (2010) Cosmetic Science in Skin Aging: Achieving the efficacy by the chitin nano-structured crystallites. SOFW-Journal, 136(3): 14-24.
32) Morganti P. (2010) Chitin Nanofibrils and their Derivatives as Cosmeceuticals. In: Se-Kwon Kim (Ed), Chitin, Chitosan, Oligosaccharides and their Derivatives. Biological Activities and Applications, New York, CRC-Press, pp. 531-542.
33) Morganti P, Del Ciotto P, Morganti G, Fabien-Soule’ V. (2011) Application of chitin nanofibrils and collagen of marine origin as bioactive ingredients. In: Se-Kwon Kim (Ed), Marine Cosmeceuticals: Latest Trends and Prospects, New York, CRC-press pp 267-289.
34) Morganti P, Fabrizi G, Tufano MA, Carezzi F, Cardillo M, Morganti G, and Nunziata ML. (2015) Green Nanotechnology Bioeconomy serving.Part1.Innovative Beauty Masks made by green nanocomposites. Poster presented at Nanotech Italy, Bologna, November, 25-27.
35) Morganti P. (2015) Bionanotechnology & Goods for a greener Planet. SOFW-Journal, 141(10):52-56.
36) Morganti P, Del Ciotto P, Stoller M, Chianese A. (2016) Antibacterial ndi Antiiflammatory green nanocomposites. In: S Pierucci and JJ Klemes (Eds), Milano. Chemical Engineering Transactions, 47: 62-66.
37) Morganti P. (2016) Unpublished data.
38) Morganti P. (2009) Chitin-Nanofibrils in skin treatment. J. Appl. Cosmetol., 27: 251-270.
39) Morganti P, Del Ciotto P, Gao Xing-Hua (2012) Skin Delivery and Controlled Release of Acive Ingredients nano encapsulated by Chitin Nanofibrils: A new approach. Cosm. Sci.Technol., 20: 136-142.
40) Morganti P. (2016) Unpublished data.
41) Aguilera B, Renkemal GH, Van der Marel GA, Ghauhharali-Van der Vlugt K, Helmond MTJ, Out JMM, Donker-Koopman WE, Grooner JEM, Boot RG, Renkeman GH, et al (2003) Transglycosidase Activity of Chitotriosidase. J. Biol. Chem., 278 (42): 40911-40916
42) Eide KB, Norberg AN, Heggset EB, Lindbom AR, Varum KM, Eijsink VGH, and Sorlie M. (2012) Human Chiotridase-Chatalyzed Hydrolysis of Chitosan. Biochemistry, 51: 487-495.
43) Ge Y, Wei Q, and Li Z. (2014) Preparation and Evaluation of the Free Radical Scavenging Activitues of Nanoscale Lignin Biomaterials. BioResources, 9(4):6699-6706.
44) Espinoza-Acosta JL, Torres-Chavez PI, Ramirez-Wong B, Lopez-Saiz CM, and Montano-Leyva B. (2016) Antioxidant, Antimicrobial, and Antimutagenic Properties of Technical Lignins and their Applications. BioResources, 11(2): 1-30.
45) Quian Y, Qiu X, and Zhu S. (2014) Lignin: a nature-inspired sun blocker for a broad-spectrum sunscreens. Green Chem., 17: 320-324.
46) Morganti P, Carezzi F, Del CiottomP, Morganti G, Nunziata ML, Gao XingHua, Chen Hong-Duo, Tischenko G, and Yudin VE. (2014) Chitin nanofibrils:A natural multifunctional polymer.Physicochemical characteristics, effectiveness and safeness. In: David Andrew Phenix and Waqar Ahmed (Eds) Nanobiotechnology, UK, One Central Press Ltd, pp1-31.
47) Morganti P. (2015) Ricerca e Sviluppo: La strada maestra per una Eco-innovazione verde. Natural1, 140: 54-57.
48) Morganti P. (2015) Green Economy and Bionanotechnology to transform waste materials in useful goods: results of EU research projects. Eurocosmetics, 22(1/2): 12-16.
49) Morganti P, Fabrizi G, Palombo M, Cardillo M, Del Ciotto P, Carezzi F. and Morganti G. (2014) Activity of Chitin Nanofibrils block-copolymers entrapping Zn/Al/SA/Allantoin on Seborrheic Dermatitis. A randomized double-blind placebo controlled study. J. Appl. Cosmetol., 32: 3-19.
50) Morganti P, Palombo M, Cardillo A, Del Ciotto P, Morganti G, and Gazzaniga G. (2012) Anti-dandruff and anti-oily efficacy of hair formulations with a repairing and restructuring activity. The positive influence of the ZN-Chitin nanofibrils complexes. J. Appl. Cosmetol., 30: 149-159
51) Mezzana P. (2008) Clinical efficacy of a New Nanofibril-based gel in wound healing. Acta Chirurgiae Investig. Dermatol., 3: 5-13.
52) Morganti P, Palombo P, Palombo M, Fabrizi G, Slovacchia F, Guevara L. and Mezzana P. (2012) A phosphatidylcholine-hyaluronic acid nanofibrils complex fir a fast skin remodelling and rejuvenation look, Clinical, Cosmetic and Investigational Dermatology, 5: 213-220.
53) Morganti P, Palombo M, Fabrizi G, Guarneri F, Slovacchia F, Cardillo A, Del Ciotto P, Carezzi F, Morganti G. (2013) New insight on anti-aging activity of chitin nanofibril-hyaluronan block copolymers entrapping active ingredients: in vitro and in vivo study. J. Appl. Cosmetol., 31: 1-29.
54) Morganti P, Del Ciotto P, Carezzi F, Guarneri F, Yip Jui Yeo (2014) Skin lightening efficacy of new formulations enhanced by chitin nanoparticles delivery system. Note I. J. Appl.
55) Morganti P, Fusco A, Paoletti I, Del Ciotto P, Palombo M, Chianese A, Baroni A, Donnarumma G. (2016) Anti-inflammatory, Immunomodulatory and Tissue Repair Activity of Human Keratinocytes by Green Innovative Nanocomposites, In print on Arc. Dermatol. Research
56) Morganti P. (2016) Unpublished data.
57) Morganti P. (2015) Bionanotechnology & Bioeconomy for a greener development. J. Appl. Cosmetol., 32: 51-65.
58) Morganti P, Chianese A and Nunziata ML. (2015) The Green Approach for Sustainable Industrial Goods, Poster presentation, SICC 40th Interdisciplinary International Concept Conference, Milano, 11-13 June.
59) Morganti P. (2015) Ricerca & Sviluppo: La strada maestra per una Eco-innovazione verde. Natural1, 140: 54-57.
60) Morganti P. ( 2014) Use of Chitin Nanofibrils from biomass for an innovative Bioeconomy. In: Jean Ebothe’ and Waqar Ahmed (Eds) Nanofabrication using Nanomaterials, Lancashire, UK, One Central Press, pp 1-22.
61) Morganti P, Del Ciotto P, Carezzi F, Nunziata ML, and Morganti G. (2016) A Chitin Nanofibril-based Non-Woven Tissue as a Medjcal Dressing: The Role of Bionanotechnology. In: Lin Y and Ging T (Eds) Nanomaterials & Regenerative Medicine, Zagreb, Criatia, IAPC Publishing, pp 123-142.

